Nur für wenige präventiv verwendete Medikamente ist ein Langzeitnutzen bei Herz-Kreislauf-Erkrankungen im Sinne einer Minderung von
Morbidität und Mortalität nachgewiesen. Dies gilt beispielsweise für Betarezeptorenblocker nach Myokardinfarkt (a-t 10 [1992], 104),1 CSE-Hemmer bei koronarer Herzkrankheit und Hypercholesterinämie (a-t 5 [1998], 47)2 sowie ACE-Hemmer und Betablocker bei Herzinsuffizienz (a-t 2 [1995], 10; 2 [1999], 21),3,4 jeweils jedoch nur für wenige, meist einen oder zwei Wirkstoffe
dieser Arzneimittelgruppen. Für später eingeführte Varianten fehlen adäquate Belege. Weitere Plazebo-kontrollierte Langzeitstudien sind ethisch
nicht mehr vertretbar. Direkte Vergleiche mit harten Endpunkten wie Morbidität und Mortalität erfordern mehrfach höhere Patientenzahlen, um
Äquivalenz nachzuweisen, als für den Beleg des Nutzens bei den Referenzarzneimitteln erforderlich waren.
Für Hersteller von Wirkstoffvarianten scheint so "der Zug abgefahren" zu sein.Um dennoch vom Markt profitieren zu können, lassen sie wenig
aufwendige Studien mit kleinen Patientenzahlen und kurzen Laufzeiten durchführen. Ziel ist, einen günstigen Einfluss auf Surrogatparameter zu
belegen, die in der pathogenetischen Kausalkette der Erkrankung eine Rolle spielen sollen. Die Übereinstimmung mit Effekten der Referenzmittel auf
Ersatzkriterien wie Blutdruck oder Lipidwerte wird dann im Sinne eines Gruppeneffekts gewertet und der gleiche Langzeitnutzen für harte Parameter
beansprucht, der jedoch nur für die bewährten Wirkstoffe dokumentiert ist.
Es besteht kein Grund, sich solcher Argumentation anzuschließen. Hersteller versuchen jedoch, besondere Anreize zu schaffen: Sie bieten Me-too-
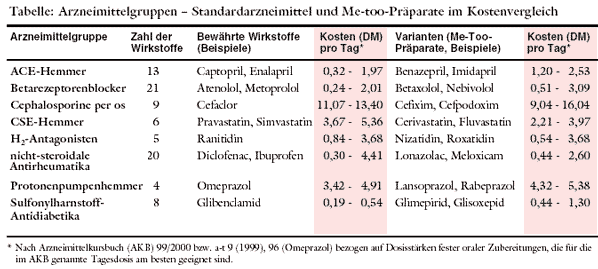
Präparate etwas preiswerter an, beispielsweise den CSE-Hemmer Fluvastatin (LOCOL; a-t 7 [1998], 66) oder den
ACE-Hemmer Imidapril (TANATRIL, s. Seite 116). Werbestrategien dienen dazu, von gemeinsamen Gruppeneffekten abzulenken:
Angebliche individuelle Vorteile der Variante werden hervorgehoben, etwa ein günstigeres Profil bei Begleitwirkungen oder bessere Verträglichkeit - ein
übliches Scheinargument bei Neueinführungen, das lediglich Ausdruck des geringen Erprobungsgrades ist (vgl. a-t 8 [1996], 77).
Triftige Gründe sprechen dagegen, den Nutzen eines gut dokumentierten Wirkstoffes pauschal auf alle Gruppenvertreter zu übertragen:
- Arzneimittelgruppen sind nicht einheitlich definiert. Sie beruhen auf chemischer Verwandtschaft (z.B. Thiazide), gleichen pharmakologischen
Wirkmechanismen (z.B. Betarezeptorenblocker) oder analoger Beeinflussung von Surrogatparametern (z.B. Antihypertensiva).5 Wirkstoffe einer Gruppe
können sich klinisch relevant unterscheiden (z.B. in Pharmakokinetik oder Rezeptorspezifität). Begleiteffekte (z.B. Endotheleffekte von Statinen, zentrale
Sympathikolyse und Einfluss auf den Kinin-Stoffwechsel bei ACE-Hemmern) können sich günstig auswirken, aber auch nachteilig (z.B. erhöhte
Fibrinogenspiegel bei CSE-Hemmern; a-t 7 [1998], 66; 8 [1998],
74).6,7 Wie sich solche Nebeneffekte langfristig klinisch auswirken, ist wenig bekannt. Sämtliche Wirkungen eines Arzneistoffs lassen sich oft
nicht überblicken. Dies gilt selbst für Jahrhundertarzneimittel wie Azetylsalizylsäure (ASPIRIN u.a.; a-t 7
[1996], 65). Es können also Unterschiede bestehen, die sich nicht einmal erfassen lassen.8
- Die Sicherheit eines Arzneimittels lässt sich nur beurteilen, wenn Daten für die Einzelsubstanz bekannt sind. Bei neuen Abkömmlingen
wird man zwar die Erfahrungen mit anderen Wirkstoffen der Gruppe heranziehen. Trotz chemischer Verwandtschaft oder gleichem Hauptwirkmechanismus kommen
dennoch selbst bei typischen Me-too-Präparaten unerwartete Störwirkungen vor, die sogar Marktrücknahmen erfordern, z.B. lebensbedrohliche
Interaktionen beim Kalziumantagonisten Mibefradil (POSICOR u.a.; a-t 7 [1998], 61), Nierenversagen beim nicht-
steroidalen Antirheumatikum Ketorolac (TORATEX; a-t 6 [1993], 61), Leberschäden beim Gyrasehemmer
Trovafloxacin (TROVAN; a-t 7 [1999], 77), Hypoglykämie, hämolytische Anämie u.a. bei Temafloxacin
(TEFLOX; a-t 6 [1992], 53) oder soeben Kardiotoxizität bei Grepafloxacin (VAXAR; s. Seite 120; a-t 3 [1998], 31). Auf Daten zur Verträglichkeit aus
Langzeitanwendungen bei großen Patientengruppen zu verzichten, bedeutet Einbußen bei der Anwendungssicherheit.
- Nur selten lassen sich günstige Langzeiteffekte einer Therapie auf der Basis von Surrogatparametern valide vorhersagen (z.B. CD4-
Zellzahl bei HIV-Infektionen).9 Häufiger hat Vertrauen auf die Validität von Surrogatparametern für den Langzeitgebrauch fatale
Folgen.10 So bessern Klasse-I-Antiarrhythmika ventrikuläre Rhythmusstörungen, erhöhen aber die Mortalität (a-t 6 [1992], 54). Positiv-inotrope Substanzen wie Flosequinan (a-t 11 [1995],
106), Xamoterol (a-t 8 [1992], 77) oder Milrinon (COROTROP; a-t 4
[1997], 45) verbessern Leistungsfähigkeit und kardiale Funktionsparameter bei Herzinsuffizienz, erhöhen aber in einigen Studien die Sterblichkeit.
Fluoride (NAFRIL RETARD u.a.) vermögen die Knochendichte deutlich zu steigern. Die Rate osteoporotischer Frakturen bleibt jedoch in einigen Studien
unverändert oder nimmt sogar zu (a-t 5 [1999], 51).
- Auch innerhalb einer Wirkstoffgruppe lässt sich der Langzeitnutzen nicht anhand von Surrogatparametern abschätzen. In Neuseeland hatte
der Ersatz von Simvastatin (belegter Nutzen für harte Endpunkte) durch das preiswertere Fluvastatin (Wirksamkeitsbeleg durch Surrogatparameter wie
Angiographiebefunde, Cholesterinsenkung) einen Anstieg vaskulärer Komplikationen zur Folge (a-t 2 [1999],
28).11 Für das Fibrat Gemfibrozil (GEVILON) ist bei Patienten mit erhöhten Triglyzerid- und niedrigen HDL-Cholesterin-Werten ein
Langzeitnutzen für klinisch relevante Endpunkte belegt.12 Bezafibrat (CEDUR u.a.) besitzt vergleichbare Effekte auf Angiographiebefunde und
Lipidwerte.13 In der Langzeitanwendung lässt sich jedoch bei gleicher Indikation keine Senkung der koronaren Morbidität und Mortalität
nachweisen.14
Nach den Vorschlägen der "Users Guides", einer Fortbildungsreihe zur Evidenz-basierten Medizin im JAMA, soll der Nutzen von Arzneimitteln im
Idealfall im direkten Langzeitvergleich mit einer Referenzsubstanz der gleichen Gruppe - bezogen auf harte Endpunkte - gemessen werden. Bei geringerem
Niveau vorhandener Studien wird jedoch auch der Nachweis einer Wirkäquivalenz auf der Basis validierter Surrogatparameter akzeptiert.5,9
Strikter beurteilen US-amerikanische Autoren die Frage der Austauschbarkeit von Arzneimitteln einer Gruppe. Sie fordern für neue Medikamente
Direktvergleiche mit Standardmitteln über längere Zeit und mit relevanten Endpunkten.8 Die Zulassung soll nur dann gewährt werden, wenn
das neue Mittel Vorteile hinsichtlich Wirksamkeit, Verträglichkeit oder bei Gleichwertigkeit zumindest Kostenvorteile bietet. Dies verringert automatisch die Zahl
verfügbarer Wirkstoffe. Eine kleine Zahl langzeiterprobter Produkte pro Arzneimittelgruppe macht Nutzen und Risiken überschaubar und reicht für die
Marktkonkurrenz aus. Planloses Ausdehnen der Palette von Statinen, ACE-Hemmern, Betablockern u.a. bringt keine relevanten Fortschritte, auch wenn solche
Pseudoinnovationen irreführend als "Schrittinnovationen" angepriesen werden.
Verschwendung personeller und ökonomischer Ressourcen blockiert die Entwicklung tatsächlich innovativer Arzneimittel.
FAZIT: Für neue Wirkstoffe einer Arzneimittelgruppe sind gleiche Wirksamkeits- und Sicherheitsnachweise wie bei Referenzsubstanzen erforderlich.
Austausch auf der Basis vermeintlicher Gruppeneffekte oder günstiger Einflüsse auf Surrogatparameter bietet keine Gewähr für positive
Langzeiteffekte, selbst wenn diese für Referenzmittel der gleichen Gruppe belegt sind. Arzneimittel, die diese Forderungen nicht erfüllen, sind
"Trittbrettfahrer". Sie dienen nicht der besseren Versorgung von Patienten, sondern dem Interesse von Herstellern, Umsätze von Teilmärkten
der Erstanbieter für sich abzuzweigen. Dem Anreiz oft nur anscheinend geringerer Kosten sollte widerstanden und statt dessen unter strikter Kosten/Nutzen-
Abwägung bewährte Substanzen ausgewählt werden, die überwiegend preiswert als Generika erhältlich sind.

|


