Unter chronisch obstruktiver Lungenerkankung (COPD) werden Emphysem, chronische (obstruktive) Bronchitis und Emphysembronchitis
zusammengefasst. Während in den USA Mortalitätsraten für kardiovaskuläre Erkrankungen sinken, steigen sie für die COPD. Hierzulande
sterben 3% bis 5% der Männer und 1% der Frauen an den Folgen. Die Krankheit lässt sich nicht heilen, die Beschwerden jedoch lindern.
Wichtigste Ursache ist das Rauchen. 90% aller COPD-Patienten sind Raucher. Die Anfälligkeit für die Erkrankung ist individuell unterschiedlich. Jeder
zweite Raucher von mindestens 20 Zigaretten pro Tag wird Symptome im Sinne einer chronischen Bronchitis entwickeln; jeder siebte eine klinisch relevante COPD.
Verglichen mit dem Einfluss des aktiven Rauchens sind andere Ursachen wie Inhalation von Stäuben oder Gasen am Arbeitsplatz, Luftverschmutzung,
Passivrauchen oder Atemwegsinfektionen in der Kindheit von untergeordneter Bedeutung.
DIAGNOSE: Die COPD beginnt schleichend. Frühe Stadien bleiben häufig unerkannt. Erste Hinweise geben wiederkehrender Husten, Auswurf,
gelegentliche Luftnot oder sich häufende Infekte der Atemwege. Zur frühzeitigen Erkennung dient die Lungenfunktionsprüfung (Spirometrie).
Entscheidender Parameter ist die forcierte Einsekundenkapazität (FEV1). Sie korreliert am besten mit der Schwere der Atemnot und dem Sterberisiko.1
Beträgt die FEV1 weniger als 70% der Vitalkapazität (VC), beweist dies eine Atemwegsobstruktion. Gleiche Werte des exspiratorischen Spitzenflusses
(PEF) bei Messungen zu verschiedenen Zeiten machen eine COPD gegenüber einem Asthma bronchiale wahrscheinlich.1 Tests zur Reversibilität
der Obstruktion mittels Betamimetika helfen bei der Therapieplanung. Radiologische oder laborchemische Untersuchungen sind routinemäßig wenig
hilfreich. Weitergehende Lungenfunktionsuntersuchungen sowie arterielle Blutgasanalysen im weiteren Krankheitsverlauf empfehlen sich in Zusammenarbeit mit
einem Pulmologen.
Die COPD wird meist anhand von FEV1 und Begleitsymptomen in drei Schweregrade eingeteilt. Die britische Leitlinie definiert 60% bis 79% der
altersentsprechenden Soll-FEV1 als milde COPD, 40% bis 59% als mittlere sowie weniger als 40% als schwere Erkrankung. Hier geht die geringste Anstrengung
bereits mit Luftnot einher.1
Therapie
Die Behandlung soll Symptome verbessern, Komplikationen verhindern, die Häufigkeit akuter Verschlechterungen verringern und die Überlebensrate
erhöhen.
Vor allem ist das Rauchen einzustellen. Dies gilt für alle Erkrankungsstadien. Die Lungenfunktion nimmt bei etwa 15% der Raucher deutlich schneller
ab als bei Nichtrauchern.1 Wird das Rauchen eingestellt, kann sich der Funktionsverlust innerhalb von Monaten auf physiologische Werte
normalisieren.2 Ex-Raucher leben länger als Patienten, die weiterrauchen.3 Der Umbau von Lungengewebe lässt sich nicht
rückgängig machen. Durch Tabakrauch ausgelöste entzündliche Veränderungen bilden sich jedoch bei Abstinenz in gewissem Umfang
zurück.4 Patienten müssen wissen, dass nur Verzicht auf Rauchen die vorzeitige Lungenschädigung aufhalten kann. Gegebenenfalls
empfehlen sich Raucherentwöhnungsprogramme sowie Nikotinersatzpräparate (a-t 2 [1999],
26).1
LEICHTE ERKRANKUNG: Die bronchodilatatorische Therapie mit Anticholinergika oder Betasympathomimetika verringert Luftnot und
erhöht die Lebensqualität, selbst wenn eine messbare Besserung der Lungenfunktion ausbleibt.5
Die inhalative Therapie wirkt schnell und wird gegenüber der Einnahme per os bevorzugt. Dosieraerosol, Pulverinhalation und Vernebler wirken gleich gut
bronchospasmolytisch.6 Vernebler sollen bei Patienten mit Schleimretention das Abhusten erleichtern und werden von einigen Betroffenen bevorzugt. Das
Anticholinergikum Ipratropiumbromid (ATROVENT u.a.) kann den Atemfluss bei Kontrollmessung nach einem Jahr im Vergleich zum Ausgangswert
verbessern, beeinflusst im weiteren Krankheitsverlauf die Abnahme der FEV1 jedoch nicht.2,7 Es gilt als Mittel der Wahl für die regelmäßige
Anwendung, da es zuverlässiger und länger wirkt als kurz wirkende Betamimetika.6 Vor allem mit lokalen Störwirkungen wie
Mundtrockenheit oder Husten ist zu rechnen.
Für die bedarfsweise Behandlung leichter COPD-Beschwerden eignen sich kurz und schnell wirkende Betamimetika wie Salbutamol
(SULTANOL u.a.). In den üblichen empfohlenen Dosierungen erweitern sie die Bronchien meist nicht maximal. In höherer Dosierung ist oft mit Tremor,
Tachykardie, Kopfschmerz und Übelkeit zu rechnen.
Nach einer systematischen Übersicht plazebokontrollierter Studien soll das lang wirkende Betamimetikum Salmeterol (SEREVENT u.a.) die
Lebensqualität verbessern.8 Der subjektiv empfundene Nutzen geht dabei nicht immer mit messbar veränderter Lungenfunktion
einher.8
In einer zwölfwöchigen Untersuchung mit 400 Patienten bessert Salmeterol Lungenfunktionsparameter stärker als Ipratropiumbromid. Auch akute
Exazerbationen sollen unter Salmeterol später auftreten. Dagegen scheint Ipratropiumbromid Atemnot deutlicher zu verringern.9 Studienmängel
schränken die Aussagekraft ein. Trotz Randomisierung haben die Patienten in der Ipratropiumbromidgruppe deutlich schlechtere FEV1-Ausgangswerte als die
der Salmeterolgruppe. Eine Intention-to-treat-Analyse* wurde nicht durchgeführt.
* |
Jeder Studienteilnehmer geht in Ergebnisberechnung ein.
|
Zu dem ebenfalls lang wirkenden Formoterol (OXIS u.a.) sind uns keine kontrollierten Studien bei COPD bekannt. Wegen des geringen
Bewährungsgrades und der möglichen Toleranzentwicklung (vgl. a-t 12 [1995], 114; 2 [1997], 18) erachten wir lang wirkende Betaagonisten derzeit als Mittel der Reserve.
MITTELSCHWERE ERKRANKUNG: Reicht Ipratropiumbromid allein nicht aus, wird üblicherweise zusätzlich ein kurz wirkender Betaagonist
empfohlen (siehe Stufenschema).1,6,10 Im kontrollierten Vergleich mit der Monotherapie bringt die Kombination indes wenig mehr:
Lungenfunktionsparameter bessern sich geringfügig, Gesamtbefinden oder Lebensqualität werden nicht beeinflusst.11 Die Kombination erscheint
somit nur vertretbar, wenn unter Monotherapie Beschwerden bestehen bleiben und die Zweifachbehandlung in einem Therapieversuch subjektive Besserung
erzielt.1
In kontrollierten Untersuchungen mit Theophyllin (SOLOSIN u.a.) allein oder in Kombination mit Bronchodilatatoren bleibt ein positiver Einfluss auf
Lungenfunktion, Sauerstoffsättigung, Belastungsfähigkeit oder Lebensqualität teilweise aus.12,13 Unabhängig von messbaren
Veränderungen berichten einzelne Anwender über subjektive Linderung von Beschwerden.12-14 Da sich diese Patienten vorab nicht erkennen
lassen, wird die versuchsweise Behandlung mit Theophyllin empfohlen, wenn unter maximaler bronchodilatatorischer Therapie noch Beschwerden bestehen. Mit
einem Auslassversuch ist der Nutzen zu prüfen.14 Störwirkungen wie Unruhe, Übelkeit, Sodbrennen oder Herzrhythmusstörungen, die
häufig schon im oberen therapeutischen Bereich (10-20 mg/l) festzustellen sind, schränken die Anwendbarkeit ein. Viele Pulmologen dosieren Theophyllin
deshalb niedriger (Blutspiegel 5-10 mg/l). Für den bronchodilatatorischen Effekt besteht jedoch eine lineare Dosis-Wirkungsbeziehung.
Orale Kortikosteroide bessern die FEV1 nur bei jedem zehnten Patienten mit stabiler COPD um mehr als 20%.15 Hoch- dosierte inhalative Steroide, z.B.
täglich 1.500 µg Beclometason (SANASTHMAX u.a.), erhöhen die FEV1 bei Patienten mit mittelschwerer COPD und nicht-reversibler Obstruktion im
Betamimetika-Test nach einer Metaanalyse von drei kleinen plazebokontrollierten Studien innerhalb von zwei Jahren geringfügig um 70 ml bis 80 ml (5 % bis 6
%).16 Nach neueren Langzeitstudien senken inhalierte Kortikosteroide in niedriger Dosierung bei leichter bis mittelschwerer Erkrankung und nicht-reversibler
Obstruktion weder die Rate von Exazerbationen, noch werden Lungenfunktion positiv beeinflusst oder Beschwerden gelindert (a-t 7 [1999], 77).17-19 In einer unveröffentlichten Studie soll täglich 1 mg Fluticason (FLUTIDE u.a.)
die Exazerbationsrate senken und die Lebensqualität erhöhen, die FEV1 jedoch nicht signifikant beeinflussen.20
Langfristiger Gebrauch von Kortikosteroiden ist nur angezeigt, wenn ein zweiwöchiger Therapieversuch den FEV1-Wert um mindestens 15% bzw. absolut um
mehr als 200 ml verbessert. Bei diesen Patienten ist zu vermuten, dass gleichzeitig eine Asthmakomponente, d.h. eine teilweise reversible Obstruktion vorliegt.
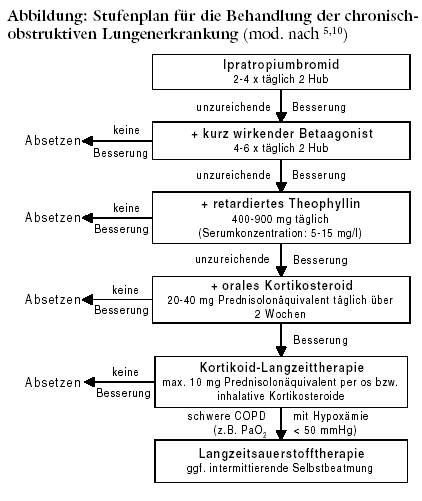
SCHWERE ERKRANKUNG: Neben Verzicht auf Rauchen erhöht nur die Langzeitanwendung von Sauerstoff die
Überlebensrate. Zwei wegweisende Studien aus den 80-er Jahren werden trotz offenen Designs als ausreichender Beleg für die Wirksamkeit
angesehen.21,22 Langfristige ambulante Sauerstoffbehandlung scheint die Mortalität bei fortgeschrittener Erkrankung (arterieller Sauerstoffpartialdruck
[PaO2] unter 50 mmHg beziehungsweise PaO2 unter 60 mmHg plus Zeichen eines chronischen Cor pulmonale oder
Polyglobulie) umso stärker zu senken, je länger sie täglich angewendet wird. Die Mindestdauer beträgt 15 bis 18 Stunden. Auch
Lebensqualität, psychische Befindlichkeit sowie neuropsychologische Testergebnisse bessern sich.21,22
Bei mittelschwerer Hypoxämie (PaO2 56 bis 65 mmHg) verringert Sauerstoff die Mortalität dagegen nicht.23 Auch
nächtliche Sauerstoffanwendung bei Patienten mit Sauerstoffmangel während des Schlafs, jedoch einem PaO2 über 60 mmHg am Tage, bleibt ohne
Einfluss auf die Sterblichkeit.24
Für Raucher kann die Sauerstofflangzeittherapie allenfalls im Ausnahmefall erwogen werden. Ein Nutzen ist wenig wahrscheinlich. Offenes Feuer in der
Nähe von Sauerstoff bedeutet zudem eine Gefahrenquelle.1,10
Arterielle Blutgasanalysen unter Sauerstofftherapie sind zur Kontrolle der Behandlung und weiteren Therapieplanung notwendig. Ein Anstieg des arteriellen
Kohlendioxidpartialdrucks (PaCO2) unter der Behandlung weist auf eine erwünschte Entlastung der Atemmuskulatur durch
Hypoventilation hin und ist mit einer günstigen Prognose verbunden.25
Erkrankte mit chronisch ventilatorischer Insuffizienz und schwerer Hyperkapnie (ab PaCO2 von 55 mmHg und mehr) durch Ermüdung
der Atemmuskulatur können mittels intermittierender Selbstbeatmung über eine Gesichts- beziehungsweise Nasenmaske behandelt werden.
Wenn eine Obstruktion und Zeichen der Hypoventilation wie Polyglobulie oder Cor pulmonale im Vordergrund stehen, scheint die Behandlung eher anzusprechen als
bei vorrangiger Emphysemproblematik. Ein Nutzen ist bislang nicht gesichert.26
Für ausgewählte Patienten, die auf Medikamente nicht ausreichend ansprechen, können chirurgische Maßnahmen wie Bullektomie bei
großen Lungenblasen oder Lungenteilresektion bei diffusem, fortgeschrittenem Emphysem erwogen werden. Prospektive Studien zur Auswahl geeigneter
Operationskandidaten und zum langfristigen Nutzen der Lungenteilresektion fehlen.27 Verlaufsuntersuchungen ausgewählter Patienten lassen
allerdings Verbesserungen von Lungenfunktionsparametern, Dyspnoe und Lebensqualität erkennen.28 Unklar ist, wie lange diese positiven Effekte
anhalten. Ultima ratio bei irreversibler hochgradiger respiratorischer Insuffizienz ist die Lungentransplantation.
UMSTRITTENE THERAPIEVERFAHREN: Für Mukolytika wird beansprucht, dass sie die Bronchialsekretion fördern, verfestigten
Bronchialschleim verflüssigen und dadurch Beschwerden sowie die Häufigkeit von Exazerbationen verringern. Nach einer systematischen Übersicht
sollen Schleimverflüssiger die Exazerbationshäufigkeit bei Patienten mit chronischer Bronchitis um 22% senken.29 Die Ausgangsrate von
fünf bis sechs akuten Verschlechterungen pro Jahr ist jedoch ungewöhnlich hoch. Ein typischer Patient mit zwei bis drei jährlichen Exazerbationen
hätte danach eine akute Verschlechterung weniger, wenn er zwei Jahre lang täglich Mukolytika einnimmt. Krankheitstage sollen sich von vier auf
dreieinhalb Tage pro Monat reduzieren. Allerdings scheint ein ungünstiger Einfluss auf den Gesamtverlauf der Erkankung möglich, da sich die FEV1, als
wichtigster prognostischer Parameter der Erkrankung, unter Anwendung von Mukolytika verschlechtern kann.29 Die Qualität der eingeschlossenen
Studien ist mäßig. So werten die meisten Untersucher ihre Daten nicht nach dem Intention-to-treat-Prinzip aus. Im internationalen Schrifttum wird der
Nutzen von Mukolytika überwiegend angezweifelt.1,6

Große Trinkmengen erleichtern das Abhusten von Auswurf nicht.30 Komplikationen wie Ödeme oder Verschlechterung eines Cor pulmonale
sind zu beachten.10,31
Seltene Ursache für ein Lungenemphysem ist der kongenitale Mangel an Alpha-1-Proteaseninhibitor (früher Alpha-1-Antitrypsin-Mangel). Für die
vorzeitige Zerstörung normalen Lungengewebes wird ein Ungleichgewicht zwischen Proteasen und Antiproteasen verantwortlich gemacht. Ein schweres
Lungenemphysem mit deutlichem Proteaseninhibitor-Mangel gilt als Indikation für die Substitution mit humanem Alpha-1-Antitrypsin-Serumkonzentrat
(PROLASTIN).10 Prospektive kontrollierte Studien zum Nutzen liegen nicht vor. Störwirkungen umfassen Fieber, Schwindel, Übelkeit,
Schüttelfrost u.a. Ein Infektionsrisiko durch das Blutprodukt scheint möglich. Wir halten die Anwendung nur im Rahmen kontrollierter Studien für
gerechtfertigt.
Nach einer Übersicht soll unter physikalischer Therapie die Fähigkeit zunehmen, Sputum abzuhusten. Lungenfunktionsparameter verändern
sich nicht. Der Stellenwert von Lungendrainage, Klopfmassage oder Vibrationstherapie bei COPD lässt sich anhand der bisher vorliegenden Untersuchungen
nicht ausreichend einschätzen.32 Der therapeutische Stellenwert des Atemphysiotherapiegeräts "Flutter" zur Sekretolyse ist unklar.
Lediglich eine plazebokontrollierte Studie bei 20 Patienten ist auffindbar. Danach soll der Flutter nach drei Monaten Lungenfunktion, Gehstrecke und Beschwerden
im Vergleich zur Scheinbehandlung bessern.33
WEITERE MASSNAHMEN: Für Patienten über 65 Jahre mit COPD (a-t 9 [1995], 90) empfiehlt sich
die Impfung gegen Virusgrippe (BEGRIVAC u.a.). Atemwegsinfekte und Gesamtsterblichkeit nehmen ab.34 Die Pneumokokkenimpfung
(PNEUMOVAX 23) wird ebenfalls vielfach empfohlen.6 Ihr Nutzen ist jedoch nicht gesichert (a-t 3 [1998],
34).1 In zwei Interventionsstudien bleibt ein Einfluss auf Pneumoniehäufigkeit, Krankenhauseinweisung und Tod aus.35,36 Nur in einer
Untersuchung schützt die Vakzine Patienten mit erhöhtem Risiko wie Lungenerkrankung, Alkoholismus oder Bettlägerigkeit vor
Pneumokokkenpneumonien.37
Pulmonale Rehabilitationsprogramme, die körperliches Training, psychologische Unterstützung und Patientenschulung einschließen,
erhöhen die Belastungstoleranz und Lebensqualität, verringern Luftnot und bessern die Selbstkontrolle über die Krankheit.38,39 Zwei Jahre
nach der Rehabilitation unterscheiden sich die Teilnehmer der Interventionsgruppe hinsichtlich Belastbarkeit und Symptomatik jedoch nicht von der
Kontrollgruppe.40 Krankengymnastische Behandlung einmal pro Monat kann Effekte einer Rehabilitation auch noch nach 18 Monaten aufrecht
erhalten.41 Alleiniges Training der Atemmuskulatur bleibt ohne Nutzen.42
KOMPLIKATIONEN: Akute Verschlechterungen einer COPD beruhen meist auf bakteriellen, zu 20% auf viralen Infektionen. Bronchodilatatoren sind
für die Zeit des Infekts höher zu dosieren. Ipratropiumbromid und Betamimetika verbessern die FEV1 gleich gut.43,44 Die additive Behandlung mit
beiden Wirkstoffgruppen hat keinen zusätzlich Nutzen.45 Dosieraerosol mit Spacer oder Vernebler bringen gleich gute Effekte.46 Für
Theophyllin lässt sich kein Nutzen absichern.31,47
Antibiotische Therapie soll Patienten vorbehalten bleiben, die unter zunehmender Atemnot leiden und größere Mengen eitrigen Sputums
produzieren.1,10 Nach einer Metaanalyse bessert sich die exspiratorische Spitzenflussrate unter Antibiose.48 Unter Scheinmedikament verschwinden die
Beschwerden seltener als unter Verum (43% versus 63%).49 Doppelt so häufig wird Therapieversagen (Krankenhauseinweisung oder zusätzliche
Antibiose) beschrieben (31% vs. 14%).49 Mittel der Wahl bei jüngeren ambulanten Patienten mit akuter Exazerbation sind Standardantibiotika wie
Amoxicillin (AMOXYPEN u.a.). Bei älteren Patienten oder Vorliegen von Risikofaktoren kommen Amoxicillin/Clavulansäure (AUGMENTAN u.a.),
Cephalosporine und nur selten Gyrasehemmer in Betracht. Bei leichter Exazerbation lässt sich abwartende Haltung rechtfertigen, sofern eine
regelmäßige ärztliche Verlaufskontrolle gewährleistet ist.43
Nach neueren plazebokontrollierten Studien können mit Beginn der Exazerbation eingenommene Kortikoide den Krankenhausaufenthalt verkürzen und
die Häufigkeit von Therapieversagen im ersten Monat verringern. Lungenfunktionsparameter bessern sich schneller als unter Plazebo.50,51 Offenbar
genügt die Einnahme von 20 mg bis 40 mg Prednisolonäquivalent pro Tag über zwei Wochen.51 Ein langfristiger positiver Effekt durch die
Steroide ergibt sich nicht.50,51
Ausreichende Flüssigkeitszufuhr bei dehydrierten Patienten ist zu gewährleisten.43 Bei respiratorischer Insuffizienz ist während der akuten
Verschlechterung Sauerstoff unter Kontrolle der Blutgase angezeigt.1 Maskenbeatmung kann die Häufigkeit von Intubationen
verringern.31,52
FAZIT: Hauptursache der chronisch obstruktiven Lungenerkrankung (COPD) ist das Rauchen. Verzicht hierauf ist der wichtigste Behandlungsschritt. Nur so
kann der beschleunigte Verlust von Lungenfunktion und der Untergang von Lungengewebe aufgehalten werden. Die einzige weitere Therapieoption, die die
Mortalität nachweislich beeinflusst, ist die langfristige Sauerstoffbehandlung bei Patienten mit schwerer COPD und ausgeprägter Hypoxämie.
Bronchodilatatoren wie Ipratropiumbromid (ATROVENT u.a.) oder Betasympathomimetika vom Typ des Salbutamol (SULTANOL N u.a.) bessern Symptome.
Routinemäßige Einnahme von Theophyllin oder Kortikosteroiden bzw. die Inhalation von Kortikoiden ist nicht angezeigt. Ihr Nutzen ist individuell durch
Auslassversuch bzw. Besserung von Lungenfunktionsparametern abzusichern. Impfung gegen Virusgrippe sowie pulmonale Rehabilitation stellen wichtige
Begleitmaßnahmen dar. Mukolytika haben keinen gesicherten Nutzen.

|



