"Blut im Stuhl-Test war gestern - Enzymtest M2-PK ist heute"1, titelt ein Schreiben der Firma ScheBo Biotech AG, die derzeit intensiv
ihren Testkit zur Darmkrebs-Vorsorgeuntersuchung bewirbt. Mit dem Stuhltest wird die von Darmtumorzellen exprimierte Tumor-M2-Pyruvatkinase nachgewiesen.
Bereits 2005 kritisierten wir, dass aussagekräftige Studien fehlen, die den Test als Screeningmethode prüfen (a-t
2005; 36: 29-30).
Anlass für die Werbekampagne ist eine aktuell unter Beteiligung von Mitarbeitern des Deutschen Krebsforschungszentrums veröffentlichte
Diagnosestudie.2 Neues bietet die Arbeit indes nicht: Wie in früheren Studien werden lediglich Messergebnisse von 65 Patienten mit kolorektalem
Karzinom denen von 917 gesunden Teilnehmern einer epidemiologischen Erhebung gegenübergestellt und daraus die Testeigenschaften des  M2-PK-Kits errechnet. M2-PK-Kits errechnet.
Die Studie erlaubt keine Aussagen zur Anwendbarkeit des Tests unter Screeningbedingungen und ist zudem mit erheblichen methodischen Mängeln behaftet:
Die Stuhlproben werden unverblindet ausgewertet und zudem in den beiden Kollektiven unterschiedlich aufbereitet. Die Auswahlkriterien der erkrankten Patienten
bleiben unklar, die Selektion der Kontrollen erscheint willkürlich.
SCREENINGUNTERSUCHUNGEN:
WIE SENSITIV? WIE SPEZIFISCH?
Bevölkerungsweite Screeningmaßnahmen (vgl. a-t 2006; 37: 115-7) haben gegenüber anderen diagnostischen Tests die Besonderheit, dass
beschwerdefreie Menschen untersucht und in Abhängigkeit von den Ergebnissen weitere diagnostische Schritte veranlasst werden. Ideal wären Tests,
die alle Erkrankten erkennen (Sensitivität = 100%) und gleichzeitig alle Gesunden als solche identifizieren (Spezifität = 100%). Solche Tests gibt es jedoch
nicht. In der Regel verhalten sich beide Testeigenschaften gegenläufig. Zwar ist es wünschenswert, durch Screening möglichst viele Erkrankte
herauszufiltern. Besonders nachteilig ist es aber dabei, wenn die Spezifität - die Fähigkeit, Gesunde als solche zu erkennen - zu niedrig ist. In einem
solchen Fall erhält eine Vielzahl gesunder Menschen ein positives Testergebnis, was üblicherweise zu weiterführender invasiver und
komplikationsträchtiger Diagnostik führt. Zudem bringt ein positives Testergebnis dann nur wenig zusätzliche Informationen, da wegen der relativen
Seltenheit der gescreenten Erkrankung viel mehr "falsch positive" als "richtig positive" Ergebnisse auftreten.
Bei einer Prävalenz der Erkrankung bei 50- bis 79-Jährigen von 1%, einer angenommenen Sensitivität von 90% sowie einer Spezifität von 75%
ergibt sich bei 1.000 Getesteten nebenstehendes Bild*. Das bedeutet: Von 10 Erkrankten werden 9 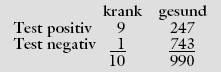 durch den Test erkannt. Allerdings kommt es auch bei 247 von 990 gesunden Testpersonen (25%) zu einem
falsch positiven Testergebnis. Nur 9 von 256 positiv Getesteten (3,5%) sind demnach tatsächlich erkrankt. Die Wahrscheinlichkeit für das Vorliegen von
Darmkrebs steigt also von 1% (Vortestwahrscheinlichkeit) auf 3,5% (Nachtestwahrscheinlichkeit). Ist das ein relevanter Zuwachs an Erkenntnis? durch den Test erkannt. Allerdings kommt es auch bei 247 von 990 gesunden Testpersonen (25%) zu einem
falsch positiven Testergebnis. Nur 9 von 256 positiv Getesteten (3,5%) sind demnach tatsächlich erkrankt. Die Wahrscheinlichkeit für das Vorliegen von
Darmkrebs steigt also von 1% (Vortestwahrscheinlichkeit) auf 3,5% (Nachtestwahrscheinlichkeit). Ist das ein relevanter Zuwachs an Erkenntnis?
Ob sich Untersuchungen als Screeningmaßnahmen eignen, lässt sich letztlich nur durch große randomisierte kontrollierte Screeningstudien mit
relevanten klinischen Endpunkten (z.B. darmkrebsbedingte Mortalität, Gesamtmortalität) belegen. Bisher ist beim Darmkrebsscreening lediglich für
den Test auf okkultes Blut im Rahmen solcher Screeningstudien eine (gleichwohl geringe) Verringerung der darmkrebsbedingten Mortalität
nachgewiesen.
* Die eingesetzten Werte für Sensitivität und Spezifität leiten wir aus den aktuellen Studien ab. Es ist möglich,
dass die Testeigenschaften bei Durchführung unter realen Screeningbedingungen schlechter ausfallen. |
Unter dem Strich kommt die Studie sogar zu ungünstigen Ergebnissen, die den Test als Screeningmethode disqualifizieren: Zwar liegt die Sensitivität
(die Fähigkeit des Tests, Kranke als Kranke herauszufiltern) bei 85%. Die Spezifität, also die Wahrscheinlichkeit, mit der das Testverfahren Gesunde auch
als solche erkennt, wird jedoch mit lediglich 79% angegeben. Jeder fünfte Gesunde weist also einen falsch positiven Test auf und müsste einer weiteren
Diagnostik, sprich Koloskopie, zugeführt werden.
Die ungünstige Beurteilung wird durch eine aktuelle prospektive Studie gestützt.3 Bei 317 Personen, die sich aus unterschiedlichen
Gründen (abdominelle Beschwerden, Vorsorge) einer Koloskopie unterziehen, wird vor der Untersuchung sowohl auf okkultes Blut als auch auf fäkales
M2-PK untersucht. Auch in dieser Studie wird zwar für den M2-PK-Test eine relativ hohe Sensitivität für die Erkennung von Kolonkarzinomen
errechnet (81%), aber eben auch eine schlechte Spezifität mit lediglich 71%.
Falsch positive Testergebnisse bei der Krebsfrüherkennung führen zu überflüssiger invasiver Folgediagnostik. Zudem sind die damit
verbundenen Befürchtungen, die zu anhaltenden Ängsten und Depression führen können, ernst zu nehmende negative
Konsequenzen.4 Ein positiver M2-PK-Test bleibt jedoch ohne Aussagekraft: Geht man davon aus, dass bei etwa 1% der Bevölkerung im Alter
zwischen 50 und 79 Jahren ein Dickdarmkrebs besteht (Prävalenz), so liegt die Wahrscheinlichkeit für das Vorliegen eines Darmkrebs bei positivem
Ergebnis mit Tumor M2-PK lediglich bei 3% bis 4% (siehe Kasten). M2-PK wird zudem nicht nur bei Darmkrebs freigesetzt: Patienten mit chronisch-entzündlichen
Darmerkrankungen, Pouchitis oder Divertikulitis sowie gesunde Raucher weisen ebenfalls erhöhte Werte auf.2,3
 Nach wie vor liegen für den Nach wie vor liegen für den  Tumor-M2-PK-Stuhltest keine randomisierten kontrollierten Screeningstudien vor. Tumor-M2-PK-Stuhltest keine randomisierten kontrollierten Screeningstudien vor.
 Nach bisherigen Daten ist die Spezifität zu gering, als dass seine
Anwendung im Rahmen von bevölkerungsweiten Screeningmaßnahmen vertretbar wäre. Nach bisherigen Daten ist die Spezifität zu gering, als dass seine
Anwendung im Rahmen von bevölkerungsweiten Screeningmaßnahmen vertretbar wäre.
 Schaden durch unnötige Folgediagnostik ist zu erwarten, der Nutzen ist
nicht belegt. Schaden durch unnötige Folgediagnostik ist zu erwarten, der Nutzen ist
nicht belegt.
| |
1 |
ScheBo Biotech AG: Schreiben vom April 2007
|
| |
2 |
HANG, U. et al.: Br. J. Cancer 2007; 96: 1329-34
|
| |
3 |
SHASTRI, Y.M. et al.: Int. J. Cancer 2006; 119: 2651-6
|
| |
4 |
JATOI, I. et al.: Breast Cancer Res. Treat. 2006; 100: 191-200
|
|

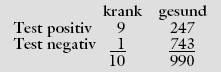 durch den Test erkannt. Allerdings kommt es auch bei 247 von 990 gesunden Testpersonen (25%) zu einem
falsch positiven Testergebnis. Nur 9 von 256 positiv Getesteten (3,5%) sind demnach tatsächlich erkrankt. Die Wahrscheinlichkeit für das Vorliegen von
Darmkrebs steigt also von 1% (Vortestwahrscheinlichkeit) auf 3,5% (Nachtestwahrscheinlichkeit). Ist das ein relevanter Zuwachs an Erkenntnis?
durch den Test erkannt. Allerdings kommt es auch bei 247 von 990 gesunden Testpersonen (25%) zu einem
falsch positiven Testergebnis. Nur 9 von 256 positiv Getesteten (3,5%) sind demnach tatsächlich erkrankt. Die Wahrscheinlichkeit für das Vorliegen von
Darmkrebs steigt also von 1% (Vortestwahrscheinlichkeit) auf 3,5% (Nachtestwahrscheinlichkeit). Ist das ein relevanter Zuwachs an Erkenntnis?