Die medikamentöse Behandlung des Morbus PARKINSON ist nach wie vor symptomatisch.1 Hauptsächlich soll die
beeinträchtigte zentrale dopaminerge Übertragung verbessert werden. In vergangenen Jahren publizierte Langzeitstudien haben die jahrzehntelange
Diskussion neu belebt, ob die Therapie der frühen PARKINSON-Erkrankung mit der Dopaminvorstufe Levodopa plus Dekarboxylasehemmer (MADOPAR u.a.)
oder mit einem Dopaminagonisten wie Ropinirol (REQUIP) begonnen werden soll (siehe Kasten).2
Mit  Rotigotin (NEUPRO) ist seit März erstmals ein Pflaster gegen M. PARKINSON auf
dem Markt, zugelassen zur Monotherapie im Frühstadium der Erkrankung.3 Wie Ropinirol und Pramipexol (SIFROL) besitzt der neue Dopaminagonist
keine Ergotaminstruktur. Die Pflasterzubereitung soll laut Werbung eine "kontinuierliche Rezeptor-Stimulation über 24 Stunden"
ermöglichen.4 Rotigotin (NEUPRO) ist seit März erstmals ein Pflaster gegen M. PARKINSON auf
dem Markt, zugelassen zur Monotherapie im Frühstadium der Erkrankung.3 Wie Ropinirol und Pramipexol (SIFROL) besitzt der neue Dopaminagonist
keine Ergotaminstruktur. Die Pflasterzubereitung soll laut Werbung eine "kontinuierliche Rezeptor-Stimulation über 24 Stunden"
ermöglichen.4
EIGENSCHAFTEN: Rotigotin besitzt Strukturähnlichkeit mit Dopamin und wirkt als Agonist an den Dopaminrezeptoren, vor allem an D3. Die lipophile
Substanz ist wegen eines hohen First-pass-Effektes per os kaum bioverfügbar. Bei transdermaler Anwendung lassen sich nach ein bis zwei Tagen stabile
Plasmaspiegel nachweisen. Rotigotin wird über verschiedene CYP-Isoenzyme metabolisiert und über Niere und Darm ausgeschieden. Die
Eliminationshalbwertszeit beträgt 5 bis 7 Stunden.3
Das nicht teilbare Pflaster ist in vier Wirkstärken erhältlich. Es wird einmal täglich gewechselt. Wegen schlechter örtlicher Verträglichkeit
darf dieselbe Applikationsstelle erst nach 14 Tagen erneut verwendet werden.3 Mehr als die Hälfte des enthaltenen Wirkstoffes verbleibt im Pflaster
und landet im Müll. Die ökologischen Folgen sind nicht hinreichend untersucht.1 Äußere Wärme im Pflasterbereich durch
übermäßiges Sonnenlicht, heiße Bäder, Sauna u.a. ist zu vermeiden. Das Pflaster muss wegen einer Aluminiumschicht vor MRT-
Untersuchungen entfernt werden.3
KLINISCHE WIRKSAMKEIT: Die beiden primär zulassungsrelevanten plazebokontrollierten Phase-III-Studien mit 277 und 561 Patienten sind nicht
vollständig veröffentlicht und somit nicht beurteilbar. In der größeren Studie wird Rotigotin zusätzlich auf Nichtunterlegenheit
gegenüber Ropinirol geprüft. Laut europäischem Beurteilungsbericht sind die im Mittel Anfang 60-jährigen, überwiegend männlichen
Patienten nicht länger als fünf Jahre an idiopathischem PARKINSON erkrankt, haben Levodopa maximal sechs Monate lang eingenommen und mit
Krankheitsstufe III nach HOEHN & YAHR* höchstens eine moderate Einschränkung erreicht. Überwiegend liegt ein geringer Schweregrad
(Stufe II nach HOEHN & YAHR) vor. Die zusätzliche konstante Einnahme von MAO-B-Hemmern wie Selegilin (MOVERGAN u.a.), Anticholinergika und
NMDA-Antagonisten wie Amantadin (PK-MERZ u.a.) ist erlaubt, Daten zum tatsächlichen Gebrauch werden nicht mitgeteilt.1
* |
HOEHN & YAHR: Stadieneinteilung der PARKINSON-Erkrankung von Stufe I bis V; Stufe III: deutliche
Bewegungsverlangsamung, beginnende Gleichgewichtsbeeinträchtigung beim Stehen oder Gehen, generalisierte moderate
Funktionsstörung.32
|
Nach einer nicht näher beschriebenen Run-in-Phase wird Rotigotin in drei bis vier Wochen bis zum Erreichen der optimalen Dosis zur Kontrolle der Symptome
auftitriert, maximal auf 6 mg bzw. 8 mg pro Tag, Ropinirol über 13 Wochen auf maximal 24 mg. Anschließend bleibt die Dosis bis zum Ende der 37. Woche
stabil.1,5 Primärer Endpunkt beider Studien ist der Anteil der "Responder" mit 20%iger Verbesserung der Aktivitäten des täglichen Lebens
und der Motorik gegenüber den Ausgangswerten, gemessen mit Teil II+III des UPDRS**. Diese wird unter Rotigotin bei 48% und 52% der Anwender erreicht
versus 19% und 30% unter Plazebo und 70% unter Ropinirol. Im Mittel nehmen die Punktwerte des UPDRS von eingangs 30 bis 33 Punkten unter Rotigotin um 4
und 7 Punkte ab gegenüber einer Senkung um 11 Punkte unter Ropinirol und einem Anstieg um 1 Punkt bzw. Abnahme um 2 Punkte unter Plazebo. Vor allem
die Motorik wird günstig beeinflusst.1
** |
UPDRS = Unified Parkinson Disease Rating Scale: Teil II (Aktivitäten des täglichen Lebens) 0-50
Punkte; III (Motorik) 108 Punkte.32
|
Der Nachweis der Nichtunterlegenheit gegenüber Ropinirol misslingt. Tatsächlich stuft die EMEA letzteres als überlegen ein.1 Zwar hat im
Ropinirol-Arm ein Drittel der Teilnehmer die Maximaldosis von 24 mg eingenommen. Doch im Rotigotin-Arm haben sogar 93% mit täglich 8 mg die höchste
zugelassene Dosis erhalten. Therapieabbrüche wegen unzureichender Wirksamkeit oder unerwünschter Effekte kommen unter der Neuerung jeweils
zumindest numerisch häufiger vor (7% vs. 4% bzw. 17% vs. 13%). Laut EMEA soll die im Vergleich zu Ropinirol geringere Wirksamkeit von Rotigotin nicht
bedenklich sein, da gegebenenfalls ein Medikamentenwechsel möglich ist.1 Während der offenen Nachbeobachtungsphasen von bis zu 18
Monaten scheint der Nutzen von Rotigotin abzunehmen.1
Für theoretische Vorteile der Pflasterzubereitung, die aus der damit verbundenen kontinuierlichen Wirkstoffabgabe abgeleitet werden, beispielsweise geringere
frühmorgendliche motorische Beeinträchtigungen oder selteneres Auftreten von Dyskinesien, fehlen aussagekräftige Belege.1
| INITIALTHERAPIE BEI MORBUS PARKINSON:
LEVODOPA ODER DOPAMINAGONISTEN?
Levodopa ist das wirksamste Medikament für die symptomatische Behandlung des M. PARKINSON.6 Auch in frühen Krankheitsstadien wirkt
es besser auf die krankheitsbedingte motorische Beeinträchtigung als Dopaminagonisten.1,7-15 Levodopa ist zudem verträglicher als diese,
beispielsweise auf Grund seltenerer gastrointestinaler oder neuropsychiatrischer Effekte.1 Problematisch sind jedoch späte
motorische Komplikationen wie Dyskinesien und/oder Fluktuationen, die unter Levodopa innerhalb von fünf Jahren bei bis zu 80% und besonders bei
jüngeren Anwendern auftreten. Sie kommen in direkten Vergleichsstudien bei Therapiebeginn mit Dopaminagonisten in den ersten Jahren seltener vor.7-
16 Daher wird diskutiert, ob initial Dopaminagonisten eingenommen werden sollten, um das Auftreten später motorischer Störwirkungen
hinauszuzögern. Offen bleibt, ob die reduzierte Inzidenz von Dyskinesien auf eine in dieser Hinsicht bessere Verträglichkeit der Dopaminagonisten
zurückzuführen ist oder auf deren geringere Wirksamkeit.17 Ohnehin benötigt die Mehrzahl der Patienten wegen des schwächeren
Effekts auch bei initialer Monotherapie mit einem neueren Dopaminagonisten in drei- bis fünfjährigen Studien zusätzlich Levodopa.7-10,15
Die Patienten der Kontrollgruppen erhalten in diesen Untersuchungen ausschließlich Levodopa. In der Praxis wird bei spät auftretenden motorischen
Störwirkungen nach Therapiebeginn mit Levodopa jedoch häufig ein Dopaminagonist ergänzt. Dennoch fehlen Untersuchungen, in denen diese
übliche Behandlungsstrategie mitgeprüft wird.2 Zur initialen Kombination beider Substanzgruppen bei frühem M. PARKINSON finden wir nur
eine größere Langzeitstudie.18
Die langfristigen Auswirkungen motorischer Komplikationen auf die Lebensqualität sind weniger gut untersucht: Im direkten Vergleich wird sie
in den ersten zwei Jahren unter Levodopa besser beurteilt als unter Pramipexol (SIFROL). Während einer nachträglich geplanten Verlängerung der
Studie um weitere zwei Jahre besteht kein signifikanter Unterschied.9,10 Motorische Komplikationen in den ersten vier Jahren verschlechtern die
durchschnittliche Lebensqualität der Patienten nicht. Sie scheinen in diesem Zeitraum überwiegend gering ausgeprägt zu sein.10,19
Für den älteren Dopaminagonisten Bromocriptin (PRAVIDEL u.a.) und Levodopa gibt es vergleichende Langzeitdaten zu motorischen Komplikationen
für 10 bis 15 Jahre: Nach 10 Jahren treten "On/Off"-Fluktuationen sowie moderate und schwere Dyskinesien bei Patienten, die initial Levodopa eingenommen
haben, nicht häufiger auf als in der Gruppe, die die Therapie mit Bromocriptin begonnen hat.12 In einer weiteren Studie haben nach 15 Jahren nahezu
alle Patienten Dyskinesien und "End-of-dose"-Phänomene erlebt, die Mehrzahl fühlt sich aber dadurch nicht wesentlich
beeinträchtigt.20
Für keine derzeit verfügbare medikamentöse Behandlung ist Neuroprotektion nachgewiesen.21,22 Früher
häufig geäußerte Befürchtungen, Levodopa beschleunige die Krankheitsprogression, sind klinisch bislang weder bestätigt noch
ausgeräumt.23 Eine große Studie, in der Patienten mit früher PARKINSON-Erkrankung 40 Wochen lang Levodopa oder Plazebo einnehmen
und sich die Symptome zwei Wochen nach Absetzen unter Verum dosisabhängig weniger stark verschlechtert haben,24 ist unseres Erachtens zu
kurz, um als Beleg für fehlende Neurotoxizität dienen zu können.
Langzeitdaten zur Mortalität liegen vor allem für den MAO-B-Hemmer Selegilin (MOVERGAN u.a.) und Bromocriptin vor,
überwiegend im Vergleich zu Levodopa. Das schwach wirksame Selegilin erhöht in einer britischen Untersuchung die Mortalität.11 Weitere
Studien und Metaanalysen bestätigen diesen Verdacht zwar nicht.14,25-8 Ein gering erhöhtes Risiko lässt sich nach einem COCHRANE
Review aber letztlich nicht ausschließen.25 Daten zur Sterblichkeit unter Bromocriptin sind widersprüchlich.16,29,30 In den drei
Langzeitstudien mit neueren Dopaminagonisten sterben unter Levodopa jeweils 2%, unter Pramipexol 1%, unter Ropinirol 3% und unter Cabergolin (CABASERIL)
4%.7,10,15 Zusätzliche Daten zu Selegilin, Dopaminagonisten und Levodopa sind von einer laufenden britischen Studie mit über 1.000 Patienten
zu erwarten.25
Während eine deutsche Konsensusleitlinie6 ähnlich wie ein älterer US-amerikanischer Behandlungsalgorithmus31 bei unter 70-
Jährigen den Therapiebeginn mit Dopaminagonisten und bei Älteren mit Levodopa favorisiert, werden diese Strategien in zwei evidenzbasierten
Leitlinien2,23 gleichberechtigt empfohlen. Unseres Erachtens kommen beide Vorgehensweisen in Betracht. Bessere Wirksamkeit und Verträglichkeit
von Levodopa bei erhöhtem Risiko später motorischer Störwirkungen sind abzuwägen gegen geringere Wirksamkeit und seltenere motorische
Effekte, aber beispielsweise häufigere neuropsychiatrische Störwirkungen von Dopaminagonisten. |
STÖRWIRKUNGEN: Mit den für Dopaminagonisten typischen Störwirkungen ist zu rechnen, beispielsweise Übelkeit (38%) und
Erbrechen (13%), Somnolenz (25%), Schwindel (18%), peripheren Ödemen (7%), orthostatischer Hypotonie (5%), Dyskinesien (3%) und Halluzinationen (2%). Sie
sollen etwa gleich häufig wie unter Ropinirol auftreten.1 Der Vergleich wird jedoch dadurch erschwert, dass die Zahlen für Rotigotin auf gepoolter
Auswertung verschiedener Dosierungen (2 mg bis 8 mg) basieren. Zusätzlich klagen 40% der Rotigotin-Anwender trotz vorschriftsmäßigen Wechsels
der Applikationsstelle über Hautreaktionen, 7% brechen deshalb die Behandlung ab.3
Die für Dopaminagonisten bekannten Schlafattacken (a-t 2000; 31: 56), unter anderem
während des Autofahrens, werden unter Rotigotin häufig (über 1%) beobachtet. Obwohl in Studien bislang nur ca. 1.100 Patienten die Neuerung
angewendet haben, sind auch Spielsucht (a-t 2005; 36: 84) und Hypersexualität (a-t 2004; 35: 36) bereits als seltene Störwirkungen beschrieben.3 Ob
Herzklappenschädigung und Pleurafibrosen (a-t 2004; 35: 52 und 1997; Nr. 8: 87-8) nur auf Ergot-Dopaminagonisten beschränkt sind, ist zur Zeit noch nicht
bekannt.1,3
Retinadegeneration bei Albinoratten ist unter Rotigotin beschrieben.1 Netzhautschäden im Tierversuch und Sehstörungen sind auch für
andere Dopaminagonisten bekannt (a-t 2005; 36: 14). Ebenso wie bei Pramipexol sollen unter Rotigotin
augenärztliche Kontrollen erfolgen.3
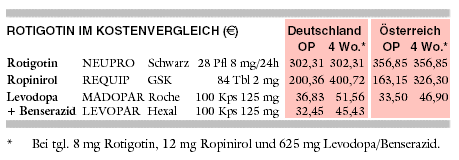
KOSTEN: Die vierwöchige PARKINSON-Therapie mit Rotigotinpflaster (NEUPRO; 8 mg/Tag) kostet 302 €. Bezogen auf eine Tagesdosis von 12
mg ist Ropinirol (REQUIP) mit 401 € ein Drittel teurer. Die Therapie mit Levodopa plus Benserazid kostet dagegen bei einer Tagesdosis von 625 mg nur etwa
ein Sechstel (MADOPAR: 52 €, LEVOPAR: 45 €).
- Mit dem nicht ergolinen Dopaminagonisten
 Rotigotin
(NEUPRO) ist erstmals ein Pflaster zur Monotherapie der frühen idiopathischen PARKINSON-Erkrankung erhältlich. Rotigotin
(NEUPRO) ist erstmals ein Pflaster zur Monotherapie der frühen idiopathischen PARKINSON-Erkrankung erhältlich.
- Die Neuerung kommt ohne vollständig veröffentlichte und damit nachvollziehbare Daten aus Phase-III-Studien auf den Markt.
- Im bis zu sechsmonatigen Vergleich wirkt Rotigotin zwar besser auf die PARKINSON-Symptomatik als Scheinmedikament, ist aber Ropinirol (REQUIP) offenbar
unterlegen. In offenen Nachbeobachtungen scheint der Effekt weiter nachzulassen.
- Für theoretische Vorteile wie verringerte frühmorgendliche motorische Beeinträchtigungen und Dyskinesien, die aus der kontinuierlichen
Wirkstofffreisetzung abgeleitet werden, fehlen aussagekräftige Belege.
- Mit den typischen Nebenwirkungen von Dopaminagonisten ist zu rechnen, zusätzlich bei 40% der Patienten mit Lokalreaktionen.
- Wir sehen derzeit keine Indikation für Rotigotin. Ob das Pflaster Patienten nützt, die trotz früher idiopathischer PARKINSON-Erkrankung bereits
an Schluckstörungen leiden, ist nicht untersucht.

|


