BEDENKLICHE NEUEINFÜHRUNG: NEUROLEPTIKUM ZIPRASIDON (ZELDOX) |
Seit Mai ist das als atypisches Neuroleptikum beworbene Ziprasidon (ZELDOX) auch in Deutschland im Handel. In den USA wurde die Zulassung 1998
wegen Sicherheitsbedenken zunächst abgelehnt. Nachdem das Mittel im zweiten Anlauf 2001 doch zugelassen wurde, müssen inzwischen bereits
Warnhinweise verschärft werden.1 Trotz allem bewirbt Pfizer das Produkt als "ausgewogen verträglich. Dafür sorgt das multifaktorielle
Verträglichkeitsprofil"2 - ein neues vom Marketing kreiertes Kriterium. EIGENSCHAFTEN: Ziprasidon hat chemisch keine Beziehung zu Phenothiazinen oder Butyrophenonen. Es blockiert sowohl Dopamin-D2- als auch Serotonin-5HT2-Rezeptoren. Es hemmt außerdem Histamin-H1- und adrenerge Alfa1-Rezeptoren sowie die Wiederaufnahme von Serotonin und Noradrenalin aus dem synaptischen Spalt.4,5 Ziprasidon wird nach Einnahme per os gut absorbiert und hauptsächlich durch Verstoffwechselung in der Leber eliminiert. An der Metabolisierung ist auch CYP3A4 beteiligt. Zwei der Hauptmetaboliten scheinen ebenfalls eine QT-verlängernde Wirkung zu haben.6 KLINISCHE WIRKSAMKEIT: Nach einer der wenigen vollständig veröffentlichten Studien wirken zweimal täglich 40 mg und 80 mg
Ziprasidon per os bei 302 Patienten mit akuter Exazerbation einer schizophrenen Psychose oder schizoaffektiven Erkrankung über sechs Wochen besser als
Plazebo.7 In einer Studie mit 139 Patienten hat nur die Tagesdosis von zweimal 60 mg im Verlauf von vier Wochen in zwei von drei primären
Endpunkten einen signifikanten Vorteil gegenüber Plazebo, nicht aber die zur Erhaltungstherapie empfohlene Dosis von zweimal 20 mg.8 Patienten mit
Therapieresistenz und relevanten EKG-Veränderungen sind von den beiden Studien ausgeschlossen. Eine weitere kleinere Studie mit 90 Patienten, in der
mehrere Ziprasidon-Dosierungen von täglich 4 mg bis täglich 160 mg mit täglich 15 mg Haloperidol (HALDOL u.a.) verglichen werden, stützt das
Behandlungsprinzip ebenfalls nicht. Hinsichtlich des primären Endpunktes ergibt sich kein Unterschied zwischen den höheren und der niedrigsten
Ziprasidon-Dosierung.3,9 
Ziprasidon darf bei bekannter Verlängerung des QT-Intervalls, nach akutem Herzinfarkt, bei nicht kompensierter Herzinsuffizienz oder
Herzrhythmusstörungen nicht verwendet werden. Die gleichzeitige Einnahme von QT-verlängernden Arzneimitteln wie Antiarrhythmika oder Malariamitteln
wie Halofantrin (HALFAN) ist kontraindiziert. Der CYP-3A4-Hemmer Ketoconazol (NIZORAL) erhöht die Serumspiegel von Ziprasidon und seinen Metaboliten,
scheint sich aber auf die QT-Verlängerung nicht auszuwirken (Tab. 1).5,6 
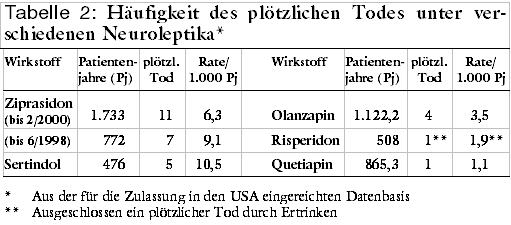
FAZIT: Das Neuroleptikum Ziprasidon (ZELDOX) scheint nach den bei der US-amerikanischen Arzneimittelbehörde FDA eingereichten Daten kardiotoxischer zu sein als andere Neuroleptika. Einen Vorteil, der das erhöhte Risiko unvorhersehbarer schwerer Herzrhythmusstörungen und des plötzlichen Herztodes aufwiegen würde, und damit einen Grund, der die Zulassung rechtfertigen würde, sehen wir nicht. Klinische Belege für "atypische" Wirkeigenschaften, insbesondere für den Nutzen bei Patienten, die auf konventionelle Therapie nicht ansprechen, sowie für ein geringeres Risiko von Spätdyskinesien, fehlen. 
|
| © 2002 arznei-telegramm |
Autor: Redaktion arznei-telegramm - Wer wir sind und wie wir arbeiten
Diese Publikation ist urheberrechtlich geschützt. Vervielfältigung sowie Einspeicherung und Verarbeitung in elektronischen Systemen ist nur mit Genehmigung des arznei-telegramm® gestattet.
