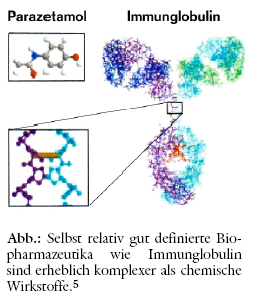
Ein solch komplexer Stoff ist auch der humanisierte monoklonale Antikörper TGN 1412 der Würzburger Firma TeGenero, der jetzt in London
bei allen sechs vormals gesunden Verum-Probanden zu lebensbedrohlichem Organversagen geführt hat. Der auch CD28-Super-MAB genannte Antikörper
soll nach den Vorstellungen der entwickelnden Firma einerseits das Immunsystem aktivieren, damit Immunzellen beispielsweise bei Blutkrebs vom B-Zell-Typ wirksam
werden können. Dabei aktiviert er T-Zellen durch Bindung an das Oberflächenmolekül CD28, ohne dass zusätzlich ein antigenspezifisches
Signal erforderlich ist. Andererseits soll TGN 1412 regulatorische T-Zellen aktivieren und damit die zu starke Immunreaktion bei Patienten dämpfen
können, die z.B. an Multipler Sklerose oder rheumatoider Arthritis erkrankt sind. Die Londoner Ereignisse machen deutlich, dass die Auswirkungen von
gentechnisch manipulierten Antikörpern auf das Immunsystem nicht so leicht kalkulierbar sind.
Phase-1-Studien mit gesunden Probanden bergen ein besonderes ethisches Problem, da die Versuchsteilnehmer - abgesehen vom Honorar, in diesem Fall jeweils
2.900 € - von der Untersuchung keinen Nutzen haben, bei grundsätzlich neuen Wirkprinzipien aber unkalkulierbare Risiken eingehen. Dies gilt
insbesondere, wenn ein Medikament, das auf ein beeinträchtigtes Immunsystem zielen soll, bei Personen mit intaktem Immunsystem geprüft wird.2
Andererseits sind besondere Risiken humanisierter Antikörper bereits aus etablierten Therapien bekannt: Zytokin-Syndrom, Capillary Leak Syndrom,
Hypersensitivitäts-Reaktionen mit Organversagen ohne auslösende Allergie. Vorbehandlung mit Glukokortikoiden zur Abschwächung solcher
Reaktionen ist in die klinische Praxis eingegangen, beispielsweise bei Therapie mit Rituximab (MABTHERA).
Im Fall TGN 1412 besteht Klärungsbedarf, ob die Erstanwendung ohne Schutzmaßnahmen zu rechtfertigen war. Die Firma TeGenero beeilte sich zwar zu
betonen, dass "alle regulatorischen und klinischen Regeln befolgt" worden seien und dass sich der Antikörper in präklinischen Studien als
sicher erwiesen habe. Auch seien die unerwünschten Effekte völlig unerwartet aufgetreten.3 Die Firma und die britische
Überwachungsbehörde, die den Probandenversuch genehmigt hat, verweigern jedoch Einblicke in die Studienprotokolle, da diese "kommerziell
sensibel" seien.3 Sowohl die genehmigende Behörde als auch die Firma dürften aber in ihren Analysen befangen sein. Geht es den
Beteiligten doch möglicherweise weniger um Aufklärung als um die Bestätigung, dass sie keine Fehler gemacht haben.
Das Argument, dass alle Vorschriften eingehalten worden seien, läuft ins Leere, wenn offen bleibt, ob die Studienprotokolle angemessen waren. Waren
Zytokin-Reaktionen und Folgezustände von der genehmigenden Behörde bedacht worden, und waren Gegenmaßnahmen eingeplant? Die Injektion
des Prüfpräparates bei allen Probanden in Abständen weniger Minuten scheint selbst bei Antikörpern, deren Auswirkungen bei Erstanwendung
unübersehbar sind, verbreitete Praxis zu sein. Ein solches Vorgehen mag die Arbeit im Auftrags-Forschungsinstitut beschleunigen, gefährdet aber die
Probanden.4 Es erscheint somit nicht akzeptabel, dass die zeitliche Abfolge der Prüfung von TGN 1412 dem Prüfinstitut überlassen worden
ist. Dies weist auf Schwachstellen in Design und Überwachung der Studie hin.
Die Verweigerung der Offenlegung gibt ein falsches Signal und schürt Misstrauen gegenüber klinischen Studien. Die Einstufung des Zulassungsdossiers
als angebliches Betriebsgeheimnis darf die unabhängige Überprüfung der Vorgänge nicht behindern. Besteht doch gerade jetzt die Chance,
durch fachöffentliche Diskussion die Verfahrensweisen von Probandenversuchen grundlegend zu überprüfen und den Anforderungen und Risiken
anzupassen, die mit den neuen Biotechnologien einhergehen. Schließlich sollen sich weltweit bereits mehr als 1.700 Biopharmazeutika in Entwicklung
befinden.5
Ethisch und rechtlich relevant ist auch die Frage, ob die Probanden hinreichend über die besonderen Risiken des Versuches, einschließlich des
Schädigungsspektrums, das von etablierten monoklonalen Antikörpern bekannt ist, aufgeklärt wurden. Auch hier darf es keine Betriebsgeheimnisse
geben. Schließlich geht es um die Gesundheit der Versuchspersonen und der nachfolgenden Patienten.
 Die Einstufung der Daten von Probandenstudien als Betriebsgeheimnis ist
nicht akzeptabel und behindert risikomindernde Maßnahmen. Die Einstufung der Daten von Probandenstudien als Betriebsgeheimnis ist
nicht akzeptabel und behindert risikomindernde Maßnahmen.
 Auf der Basis einer fachöffentlichen Auswertung der Vorgänge um
den als Superagonisten bezeichneten Antikörper TGN 1412 sollten Vertretbarkeit und Risikomanagement bei Probandenversuchen systematisch
überprüft und den heutigen Anforderungen angepasst werden. Auf der Basis einer fachöffentlichen Auswertung der Vorgänge um
den als Superagonisten bezeichneten Antikörper TGN 1412 sollten Vertretbarkeit und Risikomanagement bei Probandenversuchen systematisch
überprüft und den heutigen Anforderungen angepasst werden.
| | 1 | SELF, C.H., THOMPSON, S.: Lancet
2006; 367: 1038-9 |
| | 2 | GOODYEAR, M.: BMJ 2006; 332: 677-
8 |
| | 3 | Editorial Lancet 2006; 367:
960 |
| | 4 | COLLIER, J. zit. nach MAYOR, S.: BMJ
2006; 332: 683 |
| | 5 | ELLISON, D.E.: Scrip (Suppl.) April 2006:
14-5 |
|